Analyses histologiques et d’imagerie des macrophages synoviaux dans les modèles murins d’inflammation articulaire – Gabriel Courtiès (IRMB – Montpellier)
Intervenant
-
 Gabriel Courtiès
Gabriel CourtièsRésumé : Les maladies rhumatismales inflammatoires chroniques, telles que la polyarthrite rhumatoïde et l’arthrose, reposent sur des mécanismes cellulaires et moléculaires complexes au sein des tissus atteints. Notre équipe étudie le rôle des cellules immunitaires, et en particulier des macrophages, dans les niches tissulaires saines et pathologiques, afin de comprendre comment leurs interactions contribuent à l’inflammation, aux lésions tissulaires et aux processus de réparation.
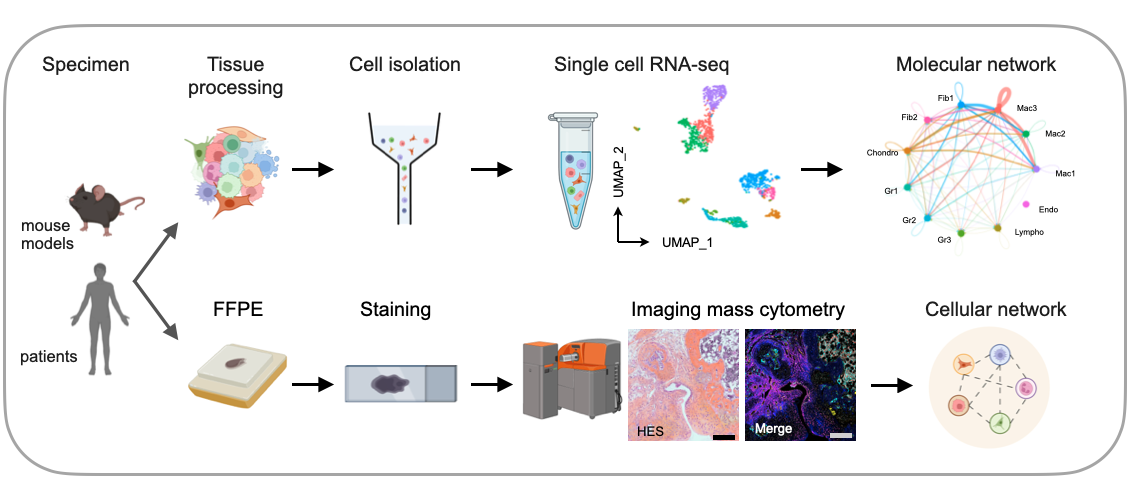
Nous nous intéressons à l’hétérogénéité des populations de macrophages (résidents et dérivés des monocytes), à leurs origines, ainsi qu’à leur organisation spatiale dans les tissus articulaires. Pour cela, nous combinons des approches de profilage transcriptionnel en cellule unique, des modèles murins de fate-mapping, la cytométrie en flux ainsi que l’histologie et l’imagerie par cytométrie de masse.
Ces stratégies permettent de cartographier les écosystèmes cellulaires impliqués dans l’inflammation articulaire, d’identifier des réseaux de communication pathologiques et d’évaluer leur remodelage sous l’effet des traitements. À terme, ces travaux visent à découvrir de nouveaux biomarqueurs de stratification et des cibles thérapeutiques pour restaurer l’homéostasie tissulaire et favoriser la résolution de l’inflammation.